Por Thais Martins
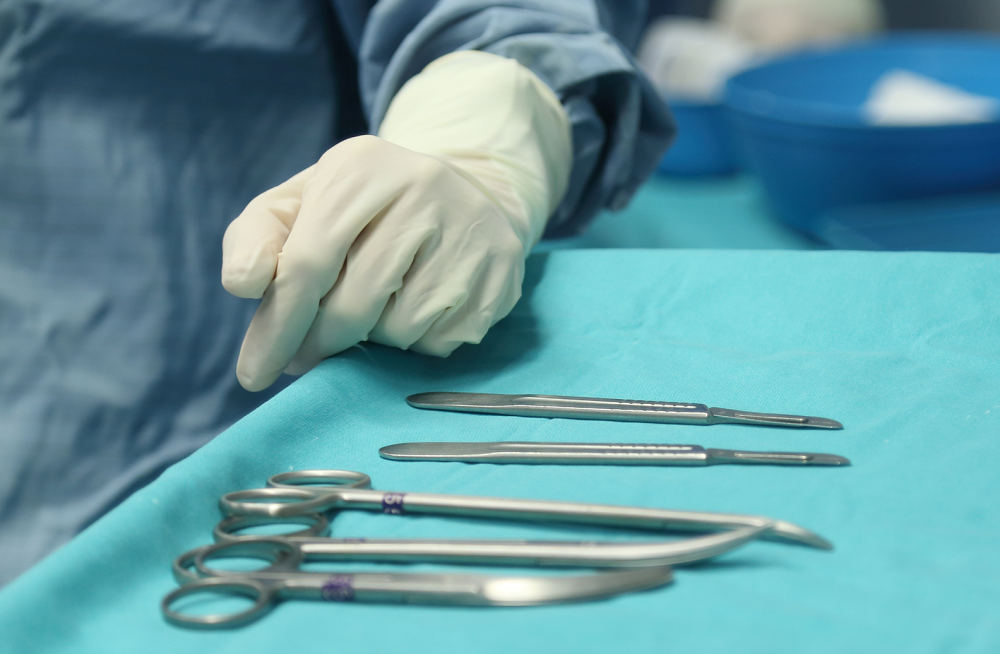
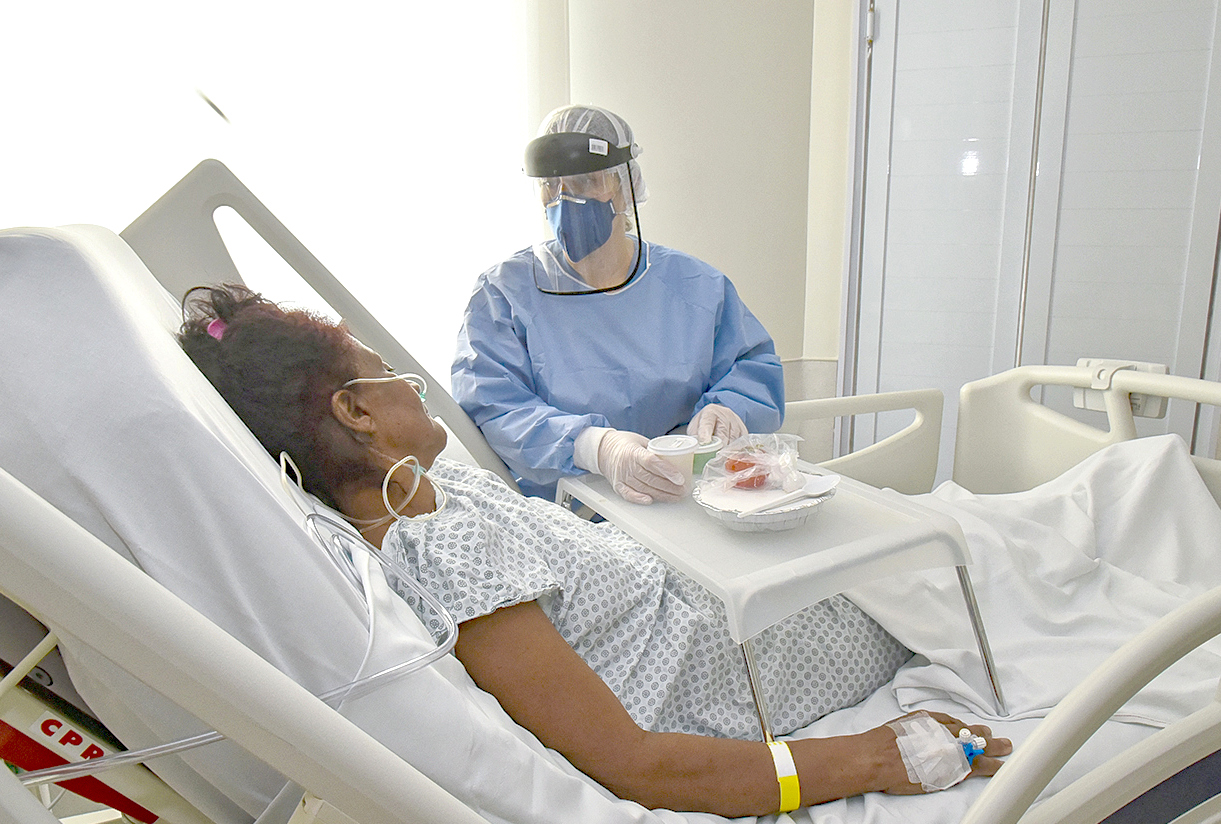
 Se o assunto é segurança, o processo de validação de equipamentos na Central de Materiais e Esterilização (CME) deve ser encarado como uma das principais etapas dentro do ambiente hospitalar. Através do processo correto de esterilização todos os parâmetros críticos devem ser analisados a fim de evitar infecções e proteger pacientes, médicos e enfermeiros, bem como os demais profissionais que operam estes equipamentos na CME.
Se o assunto é segurança, o processo de validação de equipamentos na Central de Materiais e Esterilização (CME) deve ser encarado como uma das principais etapas dentro do ambiente hospitalar. Através do processo correto de esterilização todos os parâmetros críticos devem ser analisados a fim de evitar infecções e proteger pacientes, médicos e enfermeiros, bem como os demais profissionais que operam estes equipamentos na CME.
 Vários utensílios presentes na rotina de todas as CMEs brasileiras, como as autoclaves, precisam ser validados conforme exigências da Agência Nacional de Vigilância Sanitária (Anvisa), normas da Associação Brasileira de Normas Técnicas (ABNT) e da International Organization for Standardization (ISO), além de seguir recomendações técnicas de entidades profissionais do setor voltadas à limpeza, desinfecção e esterilização de produtos para a saúde envolvidos nos processos críticos hospitalares. O objetivo principal é garantir a inativação de microrganismos causadores de contaminações e, consequentemente, a segurança dos pacientes e colaboradores presentes no dia a dia de um estabelecimento de saúde.
Vários utensílios presentes na rotina de todas as CMEs brasileiras, como as autoclaves, precisam ser validados conforme exigências da Agência Nacional de Vigilância Sanitária (Anvisa), normas da Associação Brasileira de Normas Técnicas (ABNT) e da International Organization for Standardization (ISO), além de seguir recomendações técnicas de entidades profissionais do setor voltadas à limpeza, desinfecção e esterilização de produtos para a saúde envolvidos nos processos críticos hospitalares. O objetivo principal é garantir a inativação de microrganismos causadores de contaminações e, consequentemente, a segurança dos pacientes e colaboradores presentes no dia a dia de um estabelecimento de saúde.

De acordo com Fernando Bustamante, Consultor Técnico em Esterilização da FB Cursos e Treinamentos e especialista em Gestão de Central de Material e Esterilização pela Universidad de La Coruña, na Espanha, “hoje podemos definir a validação do processo na CME como um conjunto de procedimentos para coleta e avaliação de dados, desde a fase de projeto até a limpeza, desinfecção e esterilização. Com isso, é possível estabelecer evidências e documentá-las a fim de determinar um método consistente para a entrega de produtos para saúde com qualidade”.
Para que a validação seja ainda mais eficaz, é necessário que haja qualificação. Abaixo, Bustamante enumera os motivos pelos quais é preciso qualificar, e por fim, validar os equipamentos.
- Garantir a conformidade com padrões nacionais e internacionais
- Reduzir custos
- Promover a segurança dos responsáveis pelo processo
- Promover a segurança dos pacientes
Validação em Autoclaves: seguindo as normas dos órgãos reguladores
 Conforme indica a Anvisa em sua Resolução RDC nº 15, de 15 de março de 2012, que dispõe sobre requisitos de boas práticas para o processamento de produtos para saúde e dá outras providências, no Art. 37: Deve ser realizada qualificação de instalação, qualificação de operação e qualificação de desempenho, para os equipamentos utilizados na limpeza automatizada e na esterilização de produtos para saúde, com periodicidade mínima anual.
Conforme indica a Anvisa em sua Resolução RDC nº 15, de 15 de março de 2012, que dispõe sobre requisitos de boas práticas para o processamento de produtos para saúde e dá outras providências, no Art. 37: Deve ser realizada qualificação de instalação, qualificação de operação e qualificação de desempenho, para os equipamentos utilizados na limpeza automatizada e na esterilização de produtos para saúde, com periodicidade mínima anual.
Dentro da validação de processos exigida, os profissionais da saúde devem elaborar de forma multidisciplinar um Protocolo de Qualificação da Instalação (QI), um Protocolo de Qualificação de Operação (QO) e um Protocolo de Qualificação de Desempenho (QD) para obter evidências documentadas e garantir que os processos sejam consistentes e robustos.

Sobre este mesmo assunto, Lucas Cardoso Gantus de Souza, Gerente de Serviços da Steris do Brasil, afirma que “com a validação, a CME detentora do equipamento fica em conformidade com a ONA – Organização Nacional de Acreditação (ou outro órgão acreditador), bem como com a RDC 15 da vigilância sanitária. Através da validação é possível provar que o processo de esterilização é eficaz por meio de evidências documentadas, além de otimizar e padronizar o processo de esterilização”.
“De acordo com as normas nacionais e internacionais, a validação deve ser feita no momento da instalação do equipamento, bem como a verificação para saber se o mesmo passou por alguma intervenção que possa impactar no processo, tais como troca do controlador (CLP), troca da câmara de esterilização, transferência de local, entre outros. Além disso, a requalificação deve ser feita anualmente (a cada 12 meses), assim como a calibração certificada pelo INMETRO – Instituto Nacional de Metrologia, Qualidade e Tecnologia de todos os instrumentos de medição dos itens críticos do equipamento”, completa Souza.
 Por fim, sobre os processos de validação de equipamentos como as autoclaves, ele enfatiza que por se tratar de uma verificação de todos os pontos críticos da esterilização, que são tempo, temperatura e qualidade do vapor, é imprescindível a presença do fabricante (ou uma empresa habilitada pelo mesmo) para quaisquer ajustes necessários nas parametrizações, sendo necessária também uma prévia e completa revisão preventiva no equipamento. “Como não há em nenhuma norma vigente a restrição de execução deste serviço pelo fabricante, o mesmo pode executar e garantir a qualidade nos processos da CME mantendo o equipamento calibrado e validado pelo INMETRO”, finaliza.
Por fim, sobre os processos de validação de equipamentos como as autoclaves, ele enfatiza que por se tratar de uma verificação de todos os pontos críticos da esterilização, que são tempo, temperatura e qualidade do vapor, é imprescindível a presença do fabricante (ou uma empresa habilitada pelo mesmo) para quaisquer ajustes necessários nas parametrizações, sendo necessária também uma prévia e completa revisão preventiva no equipamento. “Como não há em nenhuma norma vigente a restrição de execução deste serviço pelo fabricante, o mesmo pode executar e garantir a qualidade nos processos da CME mantendo o equipamento calibrado e validado pelo INMETRO”, finaliza.